En todo organismo las células se multiplican, nacen y mueren. Algunas lo hacen a grandes velocidades, mientras que otras lo hacen muy lentamente de acuerdo con las necesidades de los tejidos y organismos. El balance entre los procesos de nacimiento y muerte se mantiene mediante un complicado sistema de controles genéticos que involucra señales de crecimiento, de inhibición y de muerte celular. La mayoría de los cánceres se produce por daños genéticos en los componentes del sistema de controles. Al perder el control, las células se multiplican rápidamente, forman tumores, se malignizan.
El término cáncer engloba un conjunto de más de doscientas enfermedades de origen genético. La mayoría de las mutaciones se produce en las células somáticas y se transmite a las células hijas durante la mitosis. Solamente cuando la mutación se produce en el ADN de los gametos, la probabilidad de desarrollar un cáncer se hereda de padres a hijos (5, 6).
El cuerpo humano está formado por alrededor de 1014 células que se multiplican por división celular, siendo el daño o el envejecimiento la señal de que deben ser reemplazadas por células nuevas. En el normal funcionamiento del ciclo celular intervienen tres tipos de genes. Estos son los protooncogenes que participan en la formación y multiplicación normal de las células. Incluyen genes que codifican para factores de crecimiento, receptores de factores de crecimiento y todas las proteínas que intervienen en la transducción de señales de los factores de crecimiento. El protooncogén mutado se denomina oncogén, y la mutación da como resultado un aumento de la velocidad de la división celular, teniendo características autosómicas dominantes. Basta que un alelo mute para que la mutación se exprese fenotípicamente. Otros son los genes supresores de tumores, que inhiben el crecimiento celular. Pueden sufrir cambios en su ADN que disminuyan esta función, en cuyo caso las células tumorales se multiplican sin control. Se manifiestan con características autosómicas recesivas, es decir, ambos alelos tienen que estar mutados para que se expresen fenotípicamente. Entre los ejemplos de genes supresores que codifican proteínas se encuentran: a) p53 (gen que codifica la proteína tumoral 53) y b) Bcl-2 (gen que codifica la proteína 2 de la leucemia/linfoma de células B) (7). Por último, están los genes de reparación del ADN, y existen distintos mecanismos para tal fin.
Cuando los mecanismos de reparación no son suficientes o efectivos, se produce una mutación que se manifiesta como un cambio permanente en el genoma. Los destinos de una célula que ha sufrido daño genético primario son: la reparación, el aumento de la inestabilidad y la senescencia o la apoptosis; esta última funciona como un mecanismo de protección en el cual se sacrifican las células dañadas, pero el organismo prevalece.
Los sistemas de control del ciclo celular responden a información del proceso al que están controlando mediante sensores. Así, detectan que se haya completado exitosamente la replicación del ADN o que los cromosomas resultantes se hayan separado correctamente. Si por algún motivo esto no sucediera, se envían señales para retardar la progresión a la fase siguiente y para permitir que los sistemas de reparación del genoma actúen. Los puntos de control son monitoreados por proteínas inhibidoras del ciclo celular. Estas proteínas son codificadas por genes supresores de tumores, ya que su acción inhibe la división celular y promueve la reparación o la apoptosis de la célula dañada (7-9).
Las mutaciones que dan origen a células tumorales se producen con mucho mayor frecuencia en las células somáticas, por lo que no son transmisibles de progenitores a su descendencia, pero sí a las células hijas, lo que da lugar a un clon de células alteradas. Una célula tumoral se caracteriza por la pérdida de la inhibición por contacto, el aumento en la velocidad de proliferación celular, la pérdida de diferenciación (asociada a cambios metabólicos) y la formación de masas tumorales. A estas características se suman al fenotipo tumoral: inestabilidad genómica, invasión de los tejidos adyacentes, aparición de subpoblaciones migratorias, capacidad de proliferar en otros tejidos y formar metástasis, neoangiogénesis e inmortalidad celular.
El cáncer de cada persona es una combinación única de cambios genéticos. Es un proceso microevolutivo que, en general, se produce en una escala de tiempo de años, se necesitan no menos de cuatro mutaciones activantes de protooncogenes e inhibitorios de genes supresores de tumores en la misma célula para que un tumor comience a malignizarse. Dentro del mismo tumor es posible que las diversas células tengan cambios genéticos distintos (9, 10).
La carcinogénesis se divide en tres etapas: iniciación, promoción y progresión. La primera etapa es un cambio celular irreversible o mutación del ácido desoxirribonucleico que, si bien es compatible con la vida de la célula, involucra cambios en el sistema de señales bioquímicas asociadas al control de la proliferación celular o de la intercomunicación con otras células. En la segunda etapa, la célula dañada recibe estímulos para su crecimiento y proliferación y comienza a dividirse sin control. En la última, las células de las subpoblaciones que han sido generadas a partir de la expansión clonal inicial han establecido su malignidad y la enfermedad avanza (11).
Si bien el origen del cáncer es genético, la tumorigénesis surge de una interacción entre la genética y el medio ambiente. El cáncer se origina principalmente como consecuencia de la exposición prolongada a carcinógenos, entendidos como aquellos agentes químicos, físicos o biológicos que aumentan la tasa de mutación en células y tejidos específicos, y que son considerados carcinogénicos (9). Las mutaciones en el ADN pueden originarse por diversas causas, tales como los radicales libres del oxígeno (O₂), errores en la división celular, herencia, factores ambientales (exógenos y endógenos) y algunos virus (11).
La IARC (Agencia Internacional para la Investigación del Cáncer) clasificó los carcinógenos en cuatro grupos, según las pruebas científicas existentes sobre la carcinogénesis de compuestos y factores físicos (12,13), como se puede apreciar en la siguiente figura.
Figura 1. Clasificación de los carcinógenos
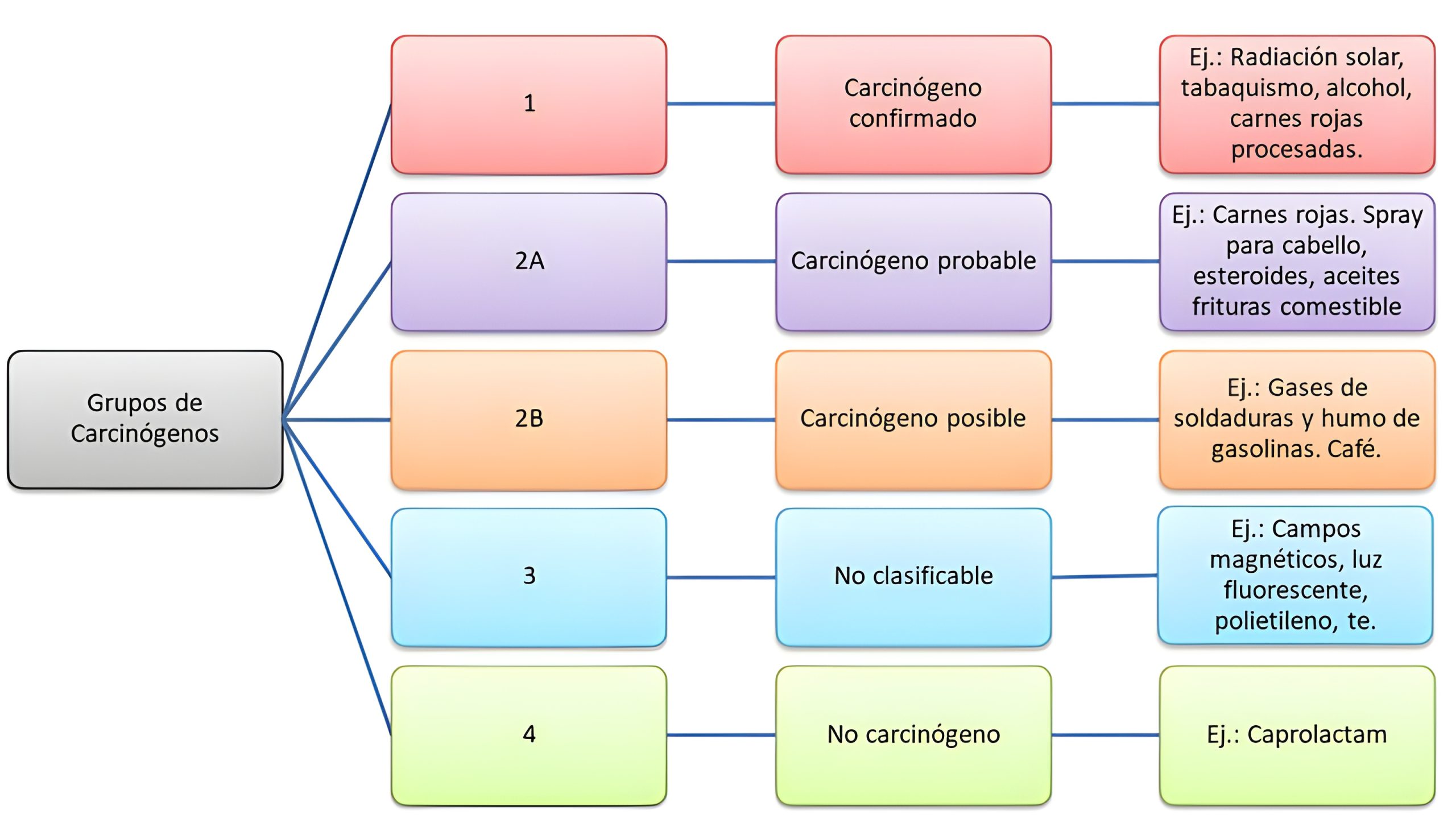
Fuente: elaboración propia con base en la referencia de la IARC, OMS.
La interacción de varios factores de riesgo contribuye al desarrollo de la enfermedad neoplásica, tal es el caso de a) factores ambientales exógenos y endógenos, y b) los factores individuales (como, por ejemplo, la predisposición genética). A través de estudios epidemiológicos, se ha demostrado que entre el 80 % y el 90 % de los tumores malignos tienen su causa en carcinógenos derivados del comportamiento humano (14).
1.1. Factores predisponentes de cáncer
Dentro del grupo de los factores predisponentes físicos se encuentran la exposición a campos electromagnéticos, radiación ionizante y radiación ultravioleta. En cuanto a los factores químicos, abarcan el alcohol, el tabaco, los compuestos organoclorados y los hidrocarburos aromáticos policíclicos (HAP). Por otro lado, los factores biológicos comprenden el sobrepeso y la obesidad, la dieta, los compuestos mutagénicos y cancerígenos presentes en los alimentos, el ejercicio físico y las infecciones.
Uno de los factores predisponentes físicos relacionados con la exposición es la presencia de campos electromagnéticos. Estos se definen como la existencia de diferencias de voltaje que, al principio, generan un campo eléctrico, el cual puede existir incluso sin corriente. Asimismo, las corrientes eléctricas son las responsables de originar los campos magnéticos. La magnitud de estos últimos varía en función del consumo de energía, mientras que la fuerza del campo eléctrico se mantiene constante.
En la vida diaria, se utilizan equipamientos que generan campos magnéticos, cuyas potencias y efectos sobre el organismo aún se desconocen. La bibliografía define que un campo magnético de 50/60 Hz puede ser un probable factor tumoral. Ejemplos de fuentes comunes incluyen ordenadores (240 Hz), televisores (200 Hz, 800 Hz, 1000 Hz), teléfonos móviles e inalámbricos (90 Hz, 120 Hz), y tecnologías como wifi o Bluetooth (2472 MHz) (11).
Existen estudios epidemiológicos que indican una relación entre la exposición a un campo magnético de baja frecuencia (entre 0 Hz y 300 Hz) y el riesgo de padecer cáncer. Se han encontrado resultados significativos que vinculan este factor a los diagnósticos de gliomas, meningiomas y leucemias (15).
La radiación ionizante también se encuentra entre los factores predisponentes físicos y se la entiende como la emisión de alta energía con la fuerza necesaria para separar un electrón de un átomo o de una molécula y causar su ionización. Se mide en Sievert (Sv), que es la unidad del Sistema Internacional de Unidades (SI) para cuantificar el efecto biológico del depósito de un joule de energía de radiación en un kilogramo de tejido humano (16, 17). Las fuentes de esta radiación pueden ser naturales, como los rayos cósmicos que atraviesan la atmósfera terrestre, o artificiales, como los equipos de imágenes médicas: radiografía, tomografía computarizada (TC) o tomografía por emisión de positrones (PET) (18).
En protección radiológica se habla de una milésima parte, es decir, en mili Sieverts (mSv). El límite de exposición que puede recibir un individuo es de 1 mSv como dosis total por año. Ejemplos de estas radiaciones son la radiografía de tórax: 0.02 mSv, la mamografía: 0.60 mSv (17). El riesgo de cáncer se incrementa en dosis de 0.5 Sv que se detectan a lo largo de los años y tienen como variables dependientes el sexo, la edad y el tipo de neoplasia que se desarrolla (19, 20).
La inducción del cáncer por medio de radiaciones ionizantes se produce por activación de los protooncogenes o por la inactivación de las células supresoras de tumores. También, por acción directa sobre el ADN o de forma indirecta por los radicales libres generados por la interacción de la radiación con el agua de la célula (21).
Los estudios diagnósticos que utilizan rayos X no implican dosis de radiación extremadamente elevadas. Se ha demostrado, epidemiológicamente, que dosis superiores a la franja entre los 50 mSv y los 100 mSv o exposiciones agudas entre 10 mSv y 50 mSv incrementan el riesgo de cáncer (17, 19, 20).
Es difícil estimar y cuantificar el daño que pueden producir dosis inferiores a 10 mSv, pero esto no significa que el riesgo sea inexistente. Este tipo de radiación puede dañar el ADN, lo que ocasionaría la formación tumoral. Así, aunque el riesgo sea bajo, si afecta a un gran número de individuos, puede resultar en un problema importante de salud pública (22, 23).
Por último, en este grupo de factores físicos se encuentra la radiación ultravioleta, definida como la exposición crónica y excesiva a la luz solar. Esta conduce a efectos adversos prematuramente, tales como eritema o quemaduras solares, envejecimiento acelerado de la piel y carcinogénesis postsolar. Se le atribuyen estos daños a la luz ultravioleta procedente del cosmos (24).
La luz se define como ondas cortas o una radiación electromagnética. Una onda corta es entendida como una perturbación o una magnitud física que varía y que se propaga en el espacio y durante el tiempo. El espectro electromagnético abarca desde las ondas de radio con longitudes de onda de kilómetros e inclusive los rayos gamma (por debajo de 0,1 nm). La luz visible es una pequeña parte del espectro.
La radiación ultravioleta, o UV, tiene una longitud de onda mayor a la de los rayos X y, a su vez, más corta que la onda de la luz visible. Estas ondas son las que implican un mayor efecto sobre las células al provocar lesiones en el ADN; debido a que su longitud de onda corta es inferior a la emitida por la luz visible. Se clasifican en tres tipos sobre la base de dicha longitud, tal como se puede observar en la gráfica siguiente (25).
Figura 2. Longitudes de onda: UV-A 320-400 nm, UV-B 280-315 nm y UB-C 200-280 nm[1]
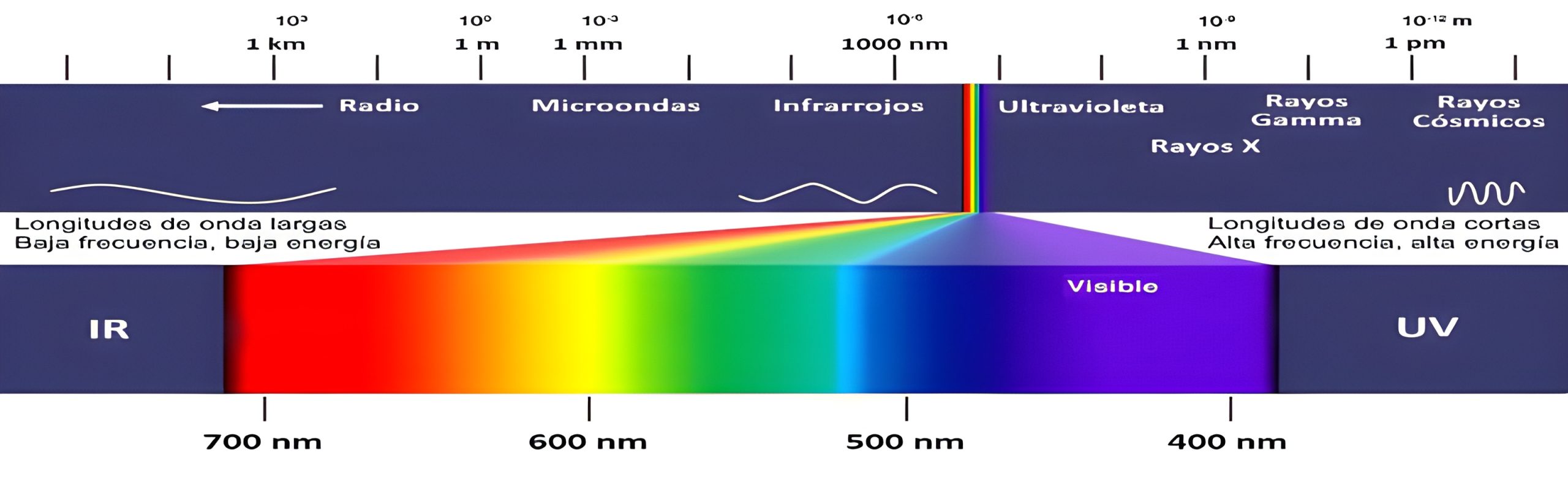
Fuente: elaboración propia.
Los efectos de esta radiación sobre la piel se miden en unidades de Dosis Estándar de Eritema (DES), las cuales equivalen a 100 J/m² (26). La radiación UV-A es la longitud de onda más cercana a la de la luz visible y sí llega a la superficie terrestre. Es capaz de generar la aparición de ERO (especies reactivas de oxígeno), como el oxígeno singlete, y favorece las lesiones como la 8-oxoguanina, que es altamente mutagénica. La exposición a esta radiación puede ser a causa del uso de lámparas en el ámbito laboral, y puede traer como consecuencia problemas oculares y cutáneos en humanos, porque al igual que la radiación UV-B (ultravioleta de onda corta) daña el ADN, de modo que se lo considera carcinógeno (27, 28).
La exposición a la radiación UV-B induce la aparición de mutaciones, así como la inmunosupresión local en la piel; también, daña las vías que permiten la inducción a la apoptosis, y promueve la proliferación de células alteradas e inmaduras. Los rayos UV-C (rayos ultravioleta de onda muy corta) tienen una longitud de onda entre 200 nm y 280 nm, por lo que son potentes y producen mucho daño a la superficie que resulta afectada.
La luz ultravioleta no solo puede ser emitida de manera externa, sino también producida artificialmente. Ejemplos de estas emisiones son las generadas por ciertas lámparas LED y, principalmente, por las camas solares, que tienen efectos cancerígenos.
Las dosis de radiación UV-A emitidas por las camas de bronceado superan los límites tolerados por la piel. Estudios sobre esta radiación UV artificial han demostrado que el uso frecuente y prolongado de solarios aumenta el riesgo de desarrollar melanoma y carcinoma escamoso de piel (27-30).
Otro grupo de factores predisponentes estudiados son los químicos, entre los que se incluyen el alcohol, el tabaco, los compuestos organoclorados y los hidrocarburos aromáticos policíclicos (HAP).
El alcohol se refiere a las bebidas alcohólicas que contienen una mezcla de diferentes sustancias, siendo el etanol la más abundante. Este compuesto es un líquido claro, incoloro, volátil e inflamable que es metabolizado por el hígado a una velocidad aproximada de entre 10 g y 15 g por hora. Su valor energético es de 7,1 kcal por gramo de alcohol.
Los mecanismos por los cuales las bebidas alcohólicas pueden ser carcinogénicas aún no están completamente determinados. Sin embargo, se atribuyen efectos genotóxicos al metabolito acetaldehído. Esta sustancia se ha establecido como un factor de riesgo para el desarrollo de carcinoma hepatocelular, carcinoma de células escamosas de esófago y cánceres de cavidad oral, faringe, laringe, colon-recto y mama (en mujeres) (31-35).
El segundo factor descripto es el tabaquismo, definido como una enfermedad adictiva crónica. La nicotina es el componente químico responsable de la adicción. Representa una de las mayores amenazas para la salud a nivel mundial. Anualmente, fallecen por esta causa unos siete millones de tabaquistas directos y un millón doscientos mil fumadores pasivos (36, 37). El tabaco sufre una combustión incompleta durante su consumo, que produce siete mil sustancias químicas, de las cuales cincuenta son cancerígenas (38, 39), entre ellas el benzopireno, que es el compuesto de mayor relevancia y un indicador principal de exposición (40, 41).
El riesgo también es mayor para los fumadores que para los exfumadores (42), siendo este hábito no solo responsable de la incidencia de cánceres como el de pulmón, sino que también eleva la mortalidad de cáncer de colon, recto y próstata (43). El hábito de fumar actúa como un carcinógeno vinculado con el virus del papiloma humano (VPH o HPV), que produce cáncer de cuello de útero (44, 45). El tabaquismo tiene una relación causal al menos con dieciséis tipos de cáncer, clasificados como tumores hematopoyéticos de laringe, riñón, vejiga, páncreas, esófago, faringe, estómago, hígado, cavidad nasal, cuello uterino, carcinoma escamoso bucal y broncopulmonar. A su vez, la evidencia demuestra que fumar puede causar cáncer de mama y leucemia en niños (35, 46).
El fumador pasivo aspira casi el 20 % del humo ambiental que exhala un fumador activo. Este humo tiene mayores concentraciones de partículas que se mantienen en suspensión, son preferentemente absorbidas por la vía aérea superior y la cavidad bucal de aquellos sujetos que estén expuestos (39, 43, 44).
Como tercer factor químico se encuentran los compuestos organoclorados, sustancias con propiedades altamente tóxicas, contaminantes ambientales permanentes y que se presentan en bajas dosis. Debido a la alta afinidad por las grasas y su baja solubilidad en el agua, se las encuentra en la grasa de las diferentes especies de animales. Las dioxinas (2, 3, 7, 8-tetraclorodibenzo-paradioxina-TCDD) y de los policlorobifenilos (PCB) (desde el 2, 3, 4, 7, 8-pentaclorodibenzofurano al PCB 126) se pueden encontrar en la carne, los lácteos, los huevos y el pescado (47-49).
Por último, se encuentran los hidrocarburos aromáticos policíclicos (HAP), un grupo de compuestos químicos muy amplio. Comúnmente se presentan en mezclas complejas, son muy abundantes en la naturaleza y son el resultado de la utilización de agroquímicos y de una combustión de hidrocarburos que reaccionan de manera incompleta con el oxígeno, lo que da como producto final monóxido de carbono y HAP.
La dieta es una fuente de exposición a estos hidrocarburos a través del consumo de alimentos cultivados en zonas contaminadas, donde los HAP están presentes en los alimentos, debido a la pirólisis (combustión incompleta) de carbohidratos, aminoácidos y ácidos grasos. El ejemplo más claro de esto sucede con el proceso de cocción de carnes a fuego directo (alta temperatura) o en los procesos de ahumado, donde se produce la formación de HAP sobre la superficie de estas (49, 50).
La medición de dichos policíclicos en diferentes estudios ha permitido establecer que la concentración aproximada que puede encontrarse en un alimento incluye entre quince y veinte tipos diferentes, siendo estas las fuentes más frecuentes de exposición en la población humana (51). Dentro de los más representativos se encuentran: acenafteno, acenaftileno, antraceno, benzo[a]antraceno; benzo[a]pireno, benzo[e]pireno, benzo[b]fluoranteno, benzo[g,h,i]perileno, benzo[j]fluoranteno, benzo[k]fluoranteno, criseno, dibenzo[a,h]antraceno, fluoranteno, fluoreno, indeno[1,2,3-c,d]pireno, fenantreno, pireno.
El benzo[a]pireno (BaP) es el más estudiado; existen límites máximos tolerables para los distintos alimentos y los procesos a los que son sometidos (1 % al 15 % del total de HAP) (52, 53). En estudios experimentales con BaP, se ha comprobado que produce mutaciones en genes supresores de tumores, como el gen p53 (54-57). Así ocurre también con el alquitrán de hulla, un subproducto que se obtiene del carbón mineral, cuando este se calienta a 1000 °C mediante pirólisis. Su uso está destinado a la producción de sustancias químicas refinadas, como el benceno, tolueno, xileno (dimetilbenceno), naftaleno y una gran variedad de compuestos aromáticos (58). El contacto con este hidrocarburo aromático y sus residuos puede ocurrir principalmente por exposición ocupacional, y es causante de cánceres de piel, pulmón, vejiga, riñón y de las vías digestivas. Además, se lo utiliza en la preparación de productos para tratar distintas afecciones de la piel, como eczema, psoriasis y caspa (59).[2]
A su vez, el benceno es un hidrocarburo aromático obtenido de la destilación del alquitrán de hulla, que se mantiene en estado líquido a temperatura ambiente y es altamente tóxico e inflamable. Se emplea en la industria como disolvente y en la fabricación de colorantes y plásticos, entre otros usos (60). La IARC estableció la carcinogenicidad de esta sustancia al asegurar que, en el cuerpo humano, es la causa del daño al sistema hematopoyético. En estudios epidemiológicos, se confirmó la relación causal entre la exposición al benceno y el desarrollo de leucemia mielógena aguda[3] (60-62).
Existen otros compuestos, como los utilizados en la industria, y en particular el uso de derivados del petróleo es una fuente importante de contaminación ambiental. De las actividades de esta categoría pueden liberarse benceno, plomo, arsénico y HAP, por lo que estos compuestos requieren actividades reguladas y controladas en cuanto a sus niveles de seguridad en la manipulación y manejo de sustancias químicas. La bioacumulación de estos tóxicos genera en la población circundante problemas endocrinos, respiratorios, inmunológicos, renales, hepáticos, alergias y malformaciones genéticas (teratógenos), entre otras afecciones (63, 64). Li et al. (65) definen la epigenética como “los factores y procesos moleculares alrededor del ADN que regulan la actividad del genoma, independientemente de la secuencia del ADN, y son mitóticamente estables”. Esta y la genética de los individuos, al exponerse a ambientes tóxicos o consumir alimentos con bioacumulación de ellos, afectan la salud humana.
Los compuestos halogenados son actualmente veintitrés contaminantes orgánicos persistentes, que incluyen las dioxinas y los insecticidas de diclorodifeniltricloroetano (DDT). Estos compuestos comparten analogía con los policlorobifenilos y la IARC los ha clasificado como carcinógenos del grupo 2A para los seres humanos. Los más estudiados son el p,p’-diclorodifenil-trichloro-etano (y su metabolito p,p’-dicloro- difenil-dicloro-etileno), el f3-hexaclorociclohexano y el hexaclorobenceno (grupo 2B-IARC), que presentan interferencia a nivel endocrino y una posible relación con el cáncer de mama y de tiroides en algunos compuestos (49, 52).
Respecto de los agroquímicos, según la bibliografía, se incluyen estudios como el de Duarte, entre otros, quien realizó una investigación en las provincias de Santa Fe, Córdoba y Entre Ríos en la cual relevó altos índices de mortalidad por cáncer en esta región de Argentina. El trabajo incluyó la correlación entre los cánceres más frecuentes en el área estudiada (pulmón, colorrectal, próstata y mama) y el trabajo agrícola e industrial (66). El auge y mantenimiento durante años del uso de los agroquímicos como organoclorados y el glifosato (N-fosfonometil) glicina tienen como característica la persistencia y la bioacumulación. Estos compuestos no tienen un proceso de descomposición rápido, lo que contribuye a su persistencia, bioacumulación y lipofilicidad. Por lo tanto, están presentes en los alimentos y contribuyen a convertirlos en factores predisponentes de enfermedades neoplásicas (64, 67).
Finalmente, la acrilamida es un hidrocarburo aromático utilizado en la industria del plástico, el papel y el tratamiento del agua potable y aguas residuales. Esta sustancia química, que es un monómero de vinilo hidrosoluble, también se encuentra en alimentos, envases de los alimentos, selladores y adhesivos. Además, forma parte del humo del tabaco.
Los alimentos que contienen carbohidratos y el aminoácido asparagina, al ser expuestos a altas temperaturas (superiores a 120 °C) y a bajas condiciones de humedad, sufren una reacción de reducción de azúcares (almidón) que provoca la descarboxilación y desaminación de la asparagina, lo que produce acrilamida como resultado final. Este proceso se conoce como reacción de Maillard. Los métodos de cocción que favorecen esta reacción son freír, asar o cocinar al horno (por ejemplo, en papas fritas, galletas, pan o café), mientras que hervir los alimentos o cocinarlos en horno microondas no genera este efecto. Un caso particular es la formación de acrilamida por pirólisis del gluten del trigo (68-70).
Los factores biológicos son los más estudiados en el ámbito de la medicina y las ciencias de la salud por su vinculación directa con el cuerpo humano. Entre ellos se incluyen el sobrepeso y la obesidad, así como la dieta, los compuestos mutagénicos y cancerígenos presentes en los alimentos, la actividad física y las infecciones.
En cuanto al sobrepeso y la obesidad, se entienden como una acumulación excesiva de grasa corporal que puede ser perjudicial para la salud. Estas condiciones se clasifican según el índice de masa corporal (IMC), y se considera sobrepeso cuando el IMC es superior a 25 y obesidad cuando supera los 30. El IMC se calcula dividiendo el peso en kilogramos por el cuadrado de la estatura en metros (IMC = peso [kg] / estatura [m]²) (71).
La obesidad se ha convertido en un problema de salud pública debido a su aumento exponencial, que ha alcanzado dimensiones pandémicas. Los sujetos con un incremento significativo en la cantidad de tejido adiposo desarrollan un estado inflamatorio crónico leve, lo que conlleva un aumento a nivel sistémico de mediadores proinflamatorios estimulados por señales de origen exógeno o endógeno. Este proceso proinflamatorio se vincula con enfermedades degenerativas crónicas, como la diabetes tipo 2, la resistencia a la insulina y las enfermedades cardíacas, así como con el daño al ADN ocasionado por el estrés oxidativo.
La inflamación provocada por el incremento del tejido adiposo favorece la infiltración y activación de macrófagos, así como el aumento en la acción de citocinas de respuesta proinflamatoria, como el factor de necrosis tumoral alfa (TNF-α), la interleucina 1-beta (IL-1β), la interleucina-12 (IL-12), el interferón-γ (IFN-γ) y la interleucina 6 (IL-6).
Además, la inflamación asociada con la obesidad favorece la tumorigénesis mediante el aumento de adipocitos hipertróficos, que estimulan la producción del factor inducible por hipoxia 1-alfa (HIF-1α) y promueven la angiogénesis (72).
En 2007, el Fondo Mundial para la Investigación del Cáncer informó que un 35 % de las incidencias de enfermedad neoplásica a nivel mundial se pueden atribuir a la obesidad y al sobrepeso. Entre los principales cánceres relacionados se encuentran el colorrectal, los cánceres de mama, de esófago, de estómago y de páncreas (73-75).
El aumento del riesgo de cáncer está más asociado a condiciones como la obesidad y a una alimentación desequilibrada, pobre en verduras y frutas, más que a la ingesta de potenciales carcinógenos en los alimentos. Sin embargo, entre los potenciales cancerígenos más importantes de la dieta se han propuesto las nitrosaminas, las aminas heterocíclicas y los hidrocarburos policíclicos aromáticos, los cuales derivan del tratamiento en la elaboración de ciertos productos alimentarios o del tipo de cocción de alimentos como las carnes (76, 77).
La dieta, relacionada con el factor predisponente anterior, es el patrón alimentario constituido por un conjunto de alimentos y productos alimentarios que una población consume de manera habitual, sea varias veces al día, a la semana o al mes. Este reúne las representaciones, creencias, conocimientos y prácticas vinculadas a la alimentación, ya sea por tradición familiar o aprendidas y compartidas por un grupo social entre sí, que se desenvuelve dentro de una cultura a lo largo de los años.
La alimentación constituye una variable multidimensional y, por tanto, medir su exposición resulta complejo, pero importante para poder evaluar los alimentos que tienen incidencia en la enfermedad neoplásica (78, 79). A partir de ella es posible observar un estilo de vida de la cultura propia de una población que vive en un hábitat con determinadas características geográficas y climáticas que limitan, en algunos casos, la disponibilidad y acceso a los alimentos y la tecnología, producción, manufactura, procesamiento, distribución y venta. Desde el proceso de globalización, se cambiaron los patrones alimentarios en gran parte de los países y culturas con prácticas poco saludables, sumado a un ritmo de vida más vertiginoso, que facilita el consumo de alimentos procesados y bajos en nutrientes.
Los alimentos ahumados, en escabeche, con alto contenido graso o calientes en extremo, debido a su pretratamiento o en su producción para el consumo, pueden contener altas dosis de nitritos y nitratos, entre los carcinógenos más importantes. Cabe destacar que se mencionan como adyuvantes en la transformación maligna el bajo consumo de calcio y vitaminas antioxidantes, así como el alto consumo de sodio. También es conocido que la dieta con alta ingesta de carnes durante toda la vida en mujeres se asocia con un aumento del 43 % en el riesgo de cáncer de mama premenopáusico (80, 81).
En la vida cotidiana, el consumo de bebidas no alcohólicas puede traer aparejados riesgos para el desarrollo de enfermedad neoplásica sin que sea tenido en cuenta. De las infusiones más conocidas, desarrollaremos el riesgo que puede resultar de un excesivo consumo de mate y de bebidas azucaradas. Estas últimas son ricas en calorías “vacías” y pueden causar aumento de peso. Las Guías Alimentarias 2020-2025 recomiendan limitar los azúcares añadidos a menos del 10 % de su ingesta diaria de calorías. Una recomendación para las mujeres es el consumo de seis cucharaditas (100 calorías) de azúcar al día, mientras que se aconseja nueve cucharaditas (150 calorías) diarias para los hombres.
El azúcar también puede encontrarse bajo diferentes nombres, como jarabe de maíz, dextrosa, fructosa, jarabe de maíz rico en fructosa, miel, sirope, sirope de agave, jarabe de arroz marrón, melaza, jugo de caña evaporado y edulcorantes no nutritivos, como el aspartamo, acesulfame K o estevia, que no aportan calorías (82).
Los riesgos asociados a la salud están dados por el aumento de peso, la resistencia a la insulina que puede derivar en diabetes tipo 2 y el incremento a padecer enfermedades cardiovasculares. Cabe recordar que en un individuo la inflamación generada por la obesidad puede desencadenar enfermedades sistémicas crónicas (83, 84).
El mate es una infusión que se prepara a base de hojas de yerba mate que se secan, cortan y muelen. Al igual que el café y el té, tiene propiedades de antimutagénico, antioxidante y antiinflamatorio. Sin embargo, debido al tratamiento previo al que deben someterse las hojas y plantas de yerba mate, se han encontrado concentraciones de HAP (benzopireno) a causa del proceso de secado (temperaturas elevadas) y procesamiento de las hojas (corte y molienda). Se ha asociado significativamente el consumo de mate con el cáncer de esófago. Los estudios realizados demuestran un nexo, aunque no hay evidencia consistente sobre la relación dosis-respuesta, es decir, asociación de mayor riesgo a mayor consumo. Por consiguiente, se considera que la relación entre la enfermedad neoplásica en el esófago y el mate puede tener dos vías: la presencia del cancerígeno benzopireno o un factor externo, como el agua caliente utilizada para el consumo de esta bebida, que genera una irritación crónica en la mucosa de este órgano (85-87).
En lo que se refiere a los compuestos mutagénicos y cancerígenos en los alimentos, entendemos por bacterias a los microorganismos unicelulares que se reproducen de forma exponencial por fisión binaria, siendo algunas de ellas patógenas o no, y son utilizadas en la industria alimenticia y farmacéutica para la elaboración de diferentes productos de consumo (yogures, antibióticos, entre otros) (88, 89).
Muchos de estos microorganismos procariontes y eucariontes (bacterias, virus, hongos) son responsables de la intoxicación alimentaria, y los signos, síntomas y gravedad dependerán del patógeno que la haya originado y del individuo que resulte afectado. La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA, por sus siglas en inglés) informa sobre las hospitalizaciones y muertes por estas causas. Los patógenos más mencionados son: a) Campylobacter jejuni, b) Clostridium perfringens, c) Clostridium botulinum, d) Escherichia coli 0157:H7, e) Listeria monocytogenes, f) virus de la hepatitis A y E, g) Bacillus Cereus, h) Shigella, i) Staphylococcus aureus, j) Vibrios (vibriosis) (90, 91).
Algunos de los compuestos mencionados, ya sean naturales o agregados por el hombre, no causan una enfermedad aguda cuando se consumen en pequeñas cantidades. Sin embargo, se acumulan en el organismo con el tiempo, lo que puede derivar en graves problemas de salud a largo plazo. Un ejemplo de ello son las micotoxinas, que producen enfermedades conocidas con el nombre de micotoxicosis. A bajos niveles, estos son carcinogénicos, mutagénicos, teratogénicos; además, producen alteraciones mitóticas, interfieren con el desarrollo fetal, pueden reducir la tasa de crecimiento y alteran la respuesta inmunológica, lo cual aumenta la susceptibilidad a infecciones. También afectan diversos órganos y sistemas, como el hígado, los riñones y los sistemas nervioso, endocrino e inmune.
Las cepas toxigénicas de hongos producen aflatoxinas, compuestos que se incluyen dentro de las micotoxinas. Estas sustancias químicas son producidas por algunas variantes del hongo filamentoso hialino y saprofito Aspergillus, como: Aspergillus flavus (B1) y Aspergillus parasiticus, Penicillium y Fusarium. Su toxicidad para humanos y ganado puede causar enfermedad y muerte. Estas toxinas se encuentran en alimentos como maíz, arroz, café, leche, legumbres, entre otros, especialmente cuando no se han tratado adecuadamente en su proceso de cosecha y comercialización. Aunque los hongos pueden ser destruidos durante los procesos industriales o de cocción, las toxinas que generan persisten en los alimentos (92, 93).
Las aflatoxinas que tienen implicancias para la salud humana son las producidas por especies de Aspergillus flavus, que generan las aflatoxinas Bl y B2 (AFBl y AFB2, respectivamente). La otra especie, el Aspergillus parasiticus, produce las aflotoxinas B, Gl y G2, Ml y M2, metabolitos de AFBl y AFB2 (pueden encontrarse en la leche). Las especies Aspergillus ochraceus y Penicillium verrucosum producen ocrotoxina A y diversas especies de Fusarium que infectan el maíz, producen fumonisinas Bl, B2 y C4 (son micotoxinas producidas por Fusarium verticillioides y F. proliferatum, que contaminan los cereales).
La aflatoxina B1 es el factor que impide el desarrollo fetal normal y tiene la mayor capacidad de carcinogénesis, dado que acelera la enfermedad. Además, este compuesto puede provocar alteraciones genéticas repentinas y permanentes, incluyendo una mutación específica en el codón 249 del gen supresor p53, lo cual está directamente relacionado con la génesis de tumores (92, 94, 95). Existen más de cuatrocientas micotoxinas, de las cuales las aflatoxinas, las ocratoxinas, las fumonisinas y la cearalenona tienen injerencia en la inducción de los cánceres de mama, hígado, esófago y próstata (96).
Es plausible que, durante el almacenamiento de granos como el maíz y el maní, así como en la producción y procesamiento de alimentos, se generen sustancias mutagénicas y cancerígenas (97, 98). Estas sustancias resultantes, que son formas activas de mutágenos, se clasifican como genotoxinas, porque se unen a la molécula del ADN, modifican sus bases y favorecen la aparición de mutaciones. Así, provocan la inactivación de genes supresores y la pérdida de la heterocigosidad (LOH, del inglés loss of heterozygosity) o la activación de protooncogenes que pueden promover la inestabilidad genómica, la aneuploidía y la transformación maligna seguida de la progresión neoplásica (99-101).
En cuanto a la actividad física, se la entiende como todo movimiento que realiza un sujeto usando los músculos esqueléticos y que permite el gasto de energía, como hacer ejercicio o practicar un deporte, realizar tareas domésticas, bailar, caminar, entre otras actividades (102). Existen estudios epidemiológicos que demuestran que, a través de diferentes mecanismos, la merma o la falta total de actividad física contribuyen de manera estrecha con la formación de tumores. Es bueno recordar que su ausencia o escasez contribuyen al sobrepeso y que este actúa alterando y aumentando la actividad endocrina (estrógenos, andrógenos, insulina y factores de crecimiento), lo que, a su vez, permite el desarrollo de tumores (103).
Luego se encuentran las infecciones, como otro factor predisponente biológico para el cáncer. En el año 2017,[4] el Instituto Nacional del Cáncer de EE. UU. afirmó que existen numerosos agentes infecciosos que contribuyen a ciertos tipos de cáncer (104, 105). De esta manera, se han identificado agentes etiológicos infecciosos, tales como las bacterias, virus, hongos y parásitos, que están asociados a las causales de cáncer. Algunos de ellos son: a) Helicobacter pylori (cáncer gástrico), b) Chlamydia pneumoniae (cáncer de pulmón), c) Chlamydia trachomatis (cáncer de cuello de útero), d) virus de Epstein-Barr (EBV) (carcinoma nasofaríngeo, linfoma de Burkitt, cáncer gástrico, linfoma de Hodgkin y cánceres de lengua y amígdalas palatinas), e) Salmonella typhi (colangiocarcinoma), f) Streptococcus bovis (cáncer colorrectal), g) Borrelia burgdorferi (linfoma), h) Human herpesvirus 8 (HHV-8) (o virus del sarcoma de Kaposi, está relacionado con el sida), i) virus del papiloma humano (VPH) (cáncer de cuello uterino, y cánceres de lengua, amígdalas y esófago), j) virus del papiloma humano T16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 y 59 (adenocarcinomas escamosos [90 %] y cervicales [75 %]), k) virus de las hepatitis B, C y D (VHB, VHC, VHD, la hepatocarcinoma primaria 80 % por VHB), l) virus del polioma de células de Merkel humano, retrovirus linfotrópico de células T humanas tipo 1 (HTLV-1) y el virus de la inmunodeficiencia humana (VIH) tipo 1 y 2 (leucemia, cáncer de pulmón y linfomas), m) Schistosoma hematobium (cáncer gástrico), n) Trematodos hepáticos (cáncer de vejiga), o) Opisthorchis viverinni y Clonorchis sinensis (colangiocarcinomas y carcinomas hepatocelulares).
En Argentina, las estimaciones realizadas en el año 2018 mostraron que cerca de diez mil casos de cáncer pueden ser atribuidos a estas infecciones (8,1 %), lo que las ubica en un lugar intermedio a nivel mundial. Con relación a Sudamérica, la IARC estimó ciento diez mil casos de cáncer atribuidos a infecciones (en el año 2018), los cuales se debieron principalmente a VPH (43,6 %) y a Helicobacter pylori (38,8 %), seguido del virus de hepatitis C (6,8%) y virus de hepatitis B (3,5%). En cuanto al sexo, el VPH explicó el 64 % de los cánceres atribuibles a infecciones en mujeres y el Helicobacter pylori explicó el 60,5 % de los cánceres atribuibles a infecciones en varones (106-108).
Por último, específicamente se hallan las hormonas utilizadas en los anticonceptivos orales. Actúan como mediadores químicos del organismo y son producidas por las glándulas endocrinas del cuerpo humano. Su transporte es a través del torrente sanguíneo a todos los componentes del cuerpo, ya sean células, tejidos, órganos (entre otros). Se definen como medicamentos del tipo hormonal, de administración por vía oral, con la finalidad de tener control sobre la natalidad, y se componen de versiones sintéticas de las hormonas femeninas naturales, que son el estrógeno y la progesterona (estrógeno y progestina).[5]
Respecto al vínculo entre el uso de anticonceptivos orales y el riesgo de desarrollar cánceres de mama, cuello de útero, endometrio, ovario, colon y recto se ha informado que efectivamente existe una asociación entre el uso de dichos anticonceptivos y los cánceres de mama y cuello uterino a largo plazo. Asimismo, se ha demostrado que el uso de esta medicación reduce los riesgos de padecer cánceres de endometrio, ovario, colon y recto (109, 110).







