Regeneración hepática
La importancia del hígado para el organismo radica en su papel esencial en el mantenimiento de la homeostasis metabólica. La amplia variedad de funciones realizadas por el hígado ha sido preservada a lo largo de la evolución al proporcionar a este órgano de una extraordinaria capacidad regeneradora en respuesta a la pérdida de su propia masa, sin que con ello resulte afectada la viabilidad del organismo.
Las células, en el hígado normal, se encuentran en estado quiescente o de reposo proliferativo. Pero, ante la pérdida de una parte de ellas, por HP o lesión hepatocelular, las células que permanecen viables experimentan un cambio rápido hacia el estado proliferativo en respuesta a determinadas señales, que se transmiten al núcleo en las etapas iniciales de la regeneración hepática y activan una serie de genes de respuesta al crecimiento. Los hepatocitos constituyen el 80-90% de las células hepáticas. El otro 20% está integrado por células de Kupffer, células endoteliales, células epiteliales biliares y células de Ito (células no parenquimatosas, NPC). La regeneración hepática tiene lugar mediante la proliferación masiva de los hepatocitos supervivientes al igual que de todas las células maduras presentes en el órgano (Michalopoulos GK, 2007).
En cuanto a los mecanismos implicados en la regeneración hepática, diversos estudios han demostrado que más de un centenar de genes participan en este proceso. El curso temporal de la expresión de esos genes define la conexión que existe entre proliferación y cese del crecimiento, e indica que se han transmitido adecuadamente las señales reguladoras de la proliferación hepatocelular en el hígado remanente (Michalopoulos GK, 2007; Su G, Guidotti H, Pezacki A, Chisari D, & Schultz E, 2002). En los humanos, la regeneración hepática ocurre luego de un daño hepático por isquemia, por inflamación causada por virus, toxinas u otras lesiones. Además, este proceso es el fundamento de aplicaciones clínicas como la remoción de un tumor de hígado, la reparación de un trauma o trasplantes con donantes vivos.
En este sentido, el conocimiento generado de este fenómeno es útil para comprender a la regeneración hepática no sólo como un resultado homeostático exitoso sino también como un proceso que puede fallar, con consecuencias catastróficas para el individuo.
Modelo experimental de hepatectomía parcial (HP)
Experimentalmente, el modelo de estudio de la regeneración hepática más utilizado es la técnica conocida como de hepatectomía parcial (HP), que consiste en la remoción quirúrgica de las 2/3 partes de la masa hepática en roedores (rata y ratón) (Higgins G & Andersson R, 1931). Dada la naturaleza multilobular del hígado de estos roedores, 3 de los 5 lóbulos hepáticos (representando 2/3 o el 70% de la masa hepática) pueden ser removidos mediante un procedimiento quirúrgico simple, sin causar daño alguno en los lóbulos residuales y sin tener asociada respuesta inflamatoria significativa ni necrosis (Michalopoulos GK, 2010). El posterior crecimiento de los lóbulos remanentes para llegar a una masa equivalente a la original se completa en 5-7 días (Michalopoulos GK, 2007). En este sentido, la regeneración hepática posterior a una HP no implica el restablecimiento de la estructura perdida, sino que se trata del crecimiento compensatorio del tejido remanente para cubrir la masa crítica funcionante (Michalopoulos GK, 2014).
Existen otros modelos experimentales para el estudio de esta función en el hígado. La injuria celular en la masa hepática puede producirse también a través de fármacos hepatotóxicos que inducen necrosis en los hepatocitos (paracetamol, CCl4, tioacetamida, etc.). Este modelo es comúnmente utilizado en investigaciones farmacológicas. En este caso, la pérdida hepática se induce por necrosis hepatocelular desencadenada en el proceso de la biotransformación del fármaco. La muerte celular está asociada a una reacción inflamatoria, que precede a la respuesta regenerativa, en la que juegan un papel importante los fagocitos residentes (células de Kupffer) y los circulantes que se activan en respuesta a la lesión, para eliminar los residuos celulares producto de la necrosis (Díez Fernández C, Boscá L, Fernández Simón L, Alvarez A, & Cascales M, 1993).
Otro modelo estudiado más recientemente, que presenta gran interés por su aplicación en la clínica, es el que se origina por embolización de la vena porta, lo que permite eliminar el riego sanguíneo portal en la porción del hígado que se va a extirpar, proporcionando mayor flujo hemodinámico a la porción restante, con la consiguiente inducción de la proliferación hepatocelular. Este modelo tiene su aplicación en casos de cirrosis, tumores y también en trasplantes de hígado de pequeño tamaño (Furrer K, Tian Y, Pfammatter T, Jochum W, El-Badry AM, Graf R, Clavien P-A, 2008).
Características de la regeneración
En los modelos de HP en roedores, luego de la cirugía se dispara una secuencia de eventos ordenados que se observan desde los primeros 5 minutos a los 5-7 días. Los hepatocitos son las primeras células en replicarse. Una HP de 2/3 deja un 1/3 de hepatocitos residuales. Éstos se someten a una ronda de síntesis de ADN, que alcanza su punto máximo a las 24 h para la rata y aproximadamente a las 36 h para el ratón. Un segundo porcentaje menor de células entra en una segunda ronda de síntesis de ADN para así restablecer el número original de hepatocitos. Una pequeña ola de apoptosis de hepatocitos es observada al final de la síntesis de ADN, lo que sugiere que es un mecanismo para corregir el disparo de una respuesta regenerativa excesiva (Sakamoto H, Liu G, Murase J, Yokomuro R, & Demetris L, 1999). La proliferación de los hepatocitos avanza desde la región periportal a las áreas pericentrales del lobulillo, como una ola de mitosis (Rabes H, 1997). De esta manera, los hepatocitos que rodean las venas centrales son los últimos en replicarse.
Además de los hepatocitos, también proliferan las NPC. Las células de Kupffer y las células epiteliales biliares proliferan aproximadamente a las 48 h post-HP y las células endoteliales alrededor de las 96 h post-HP. La médula ósea aporta progenitores para restaurar la población de estas últimas células (Wang G, Wang X, Xie G, Wang R, Hill D, & DeLeve K, 2012).
Cabe destacar que la sustitución de la masa hepática perdida está mediada por proliferación de los hepatocitos adultos maduros y otros tipos de células hepáticas, no está mediada por proliferación de una subpoblación selectiva de células madre (como en la piel y el intestino delgado). El peso del hígado se restablece aproximadamente en 5 a 7 días (8 a 15 días en humanos). Al final de la regeneración, el tamaño de los lobulillos hepáticos es notablemente más grande y el espesor de las placas de hepatocitos es casi el doble del normal (Michalopoulos GK & DeFrances R, 1997; Ogawa S, Medline F, & Farber Y, 1979). Estudios previos sugieren que se produce una lenta reorganización lobulillar durante varias semanas y, finalmente, la histología hepática se vuelve indistinguible de la original (Wagenaar Y, Chamuleau J, Pool, de Haan Q, Maas R, & Korfage K, 1993).
En términos generales, la HP es un tipo de lesión hepática, aunque no da como resultado ningún daño histológico inmediato. Por lo tanto, no es sorprendente que las vías de señalización que se activan durante la regeneración del hígado se parecen mucho a las de la cicatrización de heridas, observadas en otros tejidos. La diferencia con el proceso clásico de cicatrización de heridas es que los cambios observados en el hígado ocurren en todo el órgano.
Vías de señalización implicadas en la regeneración hepática posterior a una HP
Una característica importante de la regeneración hepática es la redundancia de vías de señalización que actúan en el proceso, es decir que, si cierta proteína o gen se afecta, la regeneración se ve retrasada pero no interrumpida, dado las múltiples vías que actúan y pueden compensar la falta de determinada señalización.
El proceso de regeneración hepática en general puede ser dividido en una fase de preparación (0-6 h post-HP), una fase proliferativa (12-72 h post-HP) y una fase terminal (120-168 h post-HP) (Michalopoulos GK, 2007). Se pueden distinguir dos clases de genes: los que regulan el crecimiento, elevando su expresión durante la fase proliferativa y retornando a su expresión normal a los 3 días de la HP, y los que regulan el ciclo celular, mostrando un máximo a las 24-36 h, que coincide con la primera ronda de replicación del ADN, seguido de una segunda ronda menos intensa a las 48 h de la hepatectomía. Parte de estos genes son los denominados genes tempranos inmediatos y otro número de ellos se expresa pocas horas después de la inducción de los genes tempranos inmediatos, y son los genes denominados genes tempranos retrasados, los cuales se regulan a nivel transcripcional o post transcripcional por los productos de los genes tempranos inmediatos. Respecto a esto, una cascada reguladora de la expresión de genes del ciclo celular permite a la célula progresar a través de la fase G1 del ciclo. Los cambios en los niveles de ciclinas y sus quinasas, por regulación transcripcional y post transcripcional, permite la transición G1 (ciclina D, CDK4 y 6) hasta S (ciclina E, CDK2), y por las últimas fases del ciclo celular, G2/M (ciclinas A, B, CDK1). Los complejos ciclina D/CDK4 y 6 están implicados en la progresión a través del punto de restricción en G1. Los inhibidores asociados a las ciclinas, p21 y p27, son importantes tanto por su intervención a través del ciclo como por su inhibición en caso de proliferación alterada (figura 1) (Kim S, Mars R, Stolz LR, Petersen JP, & Michalopoulos GK, 1997)
Ciclo celular de las células hepáticas luego de una HP

Figura 1: Ciclo celular de las células hepáticas luego de una HP. Las células normales quiescentes en G0, sufren una rápida transición a G1 que va acompañada por la transcripción de genes tempranos inmediatos de respuesta al crecimiento, seguida por la de los genes tempranos retrasados y por las ciclinas. A continuación, las células sufren la replicación del ADN en la fase S y posteriormente la transición G2/M, que implica la entrada en mitosis.
De forma general, la regeneración hepática depende en gran medida de las interacciones entre hepatocitos, NPC y otras células extrahepáticas. Dichas células producen citoquinas que incluyen el factor de necrosis tumoral α (TNF-α, del inglés tumor necrosis factor α) y la interleuquina-6 (IL-6), factores de crecimiento tales como el factor de crecimiento de hepatocitos (HGF, del inglés hepatocyte growth factor), el factor de crecimiento epidérmico (EGF, del inglés epidermal growth factor), el factor de crecimiento transformante α (TGF-α, del inglés transforming growth factor α), la insulina y el glucagón. También intervienen en el proceso distintas quinasas de señalización intracelular, factores de transcripción y otras proteínas (Michalopoulos GK, 2007).
Posterior a una HP, los hepatocitos maduros (quiescentes) rápidamente entran en el ciclo celular para recuperar el volumen hepático. Se estima que dentro de las 48 h post-HP, el 95% de los hepatocitos están proliferando y que los mismos participan en 1 o 2 vueltas de proliferación celular para restablecer la masa hepática (Michalopoulos GK, 2014). Los hepatocitos son las primeras células que entran en el ciclo celular y proliferan. Luego de producida la HP, señales extracelulares muy tempranas estimulan la proliferación de los hepatocitos: el TNF-α y la IL-6 son liberados por las células de Kupffer inmediatamente después de la HP y contribuyen al inicio del ciclo celular (de G0 a G1) al unirse a sus receptores y activar sus vías de señalización. IL-6 media su señalización a través de la activación del factor de transcripción STAT3, mientras que la señalización de TNF-α se asocia con una rápida activación del factor de transcripción NF-κB (Fausto A, Campbell B, & Riehle H, 2006). A su vez, la activación de NF-κB induce la producción de IL-6 tanto por parte de las células de Kupffer como de los hepatocitos (Taub A, 2004).
Otra de las vías importantes que actúa temprano en la regeneración hepática es la vía Wnt canónica, la cual actúa a través de la proteína β-catenina. Se ha demostrado que los principales ligandos Wnts que actúan en regeneración son Wnt2 y 9, que provienen de las células endoteliales y de las células de Kupffer y estimulan la señalización por β-catenina en los hepatocitos (Preziosi M, Okabe H, Poddar, Singh SP, & Monga S, 2018). Posteriormente, factores de crecimiento como el HGF, el EGF y el TGF-α estimulan la replicación del ADN y la mitosis. Además de los hepatocitos, también proliferan las células epiteliales biliares que inician su síntesis de ADN inmediatamente después de que lo hacen los hepatocitos y las células endoteliales sinusoidales, las cuales proliferan mediante un proceso que es más prolongado y complicado y que incluye el aporte de progenitores endoteliales desde la médula ósea al hígado (Wang G, Wang X, Xie G, Wang R, Hill D, & DeLeve K, 2012). De un modo similar, la médula ósea también aporta progenitores para restaurar la población de células de Kupffer.
En resumen, el circuito esencial requerido para la regeneración hepática está comprendido por tres tipos de vías: la de las citoquinas, la de los factores de crecimiento y también vías metabólicas que conectan la función hepática con el crecimiento celular y la proliferación. El proceso de regeneración hepática requiere de la acción de estas múltiples vías, que no son independientes y que presentan redundancia entre los componentes intracelulares de las mismas, de modo de que la pérdida de un gen individual raramente conduce a la inhibición completa de la regeneración (Fausto A, Campbell B, & Riehle H, 2006).
Principales factores involucrados en la regeneración hepática
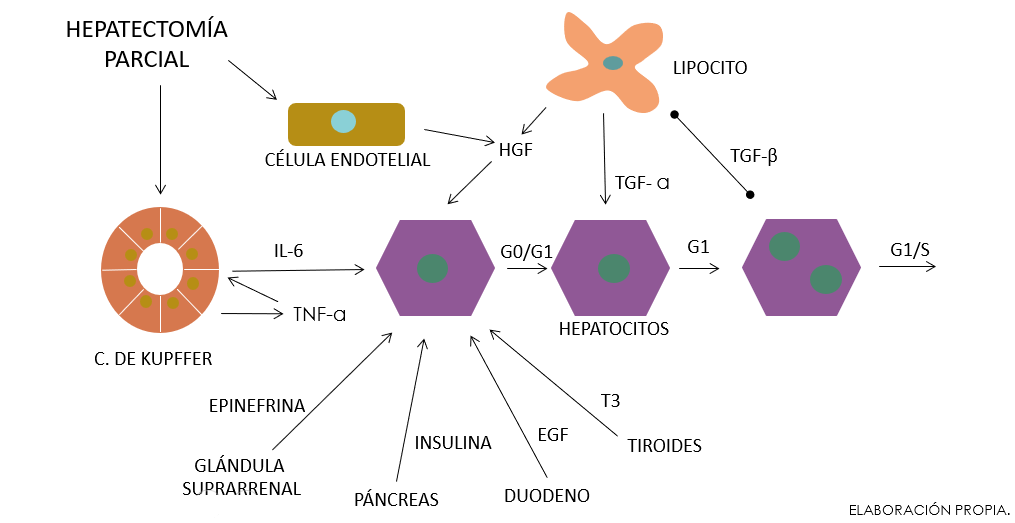
Si bien la totalidad de las vías de señalización que participan de cada fase durante el proceso de regeneración del hígado aún no se conocen en detalle, los factores implicados en la respuesta a la HP se han clasificado en cinco categorías basadas en el modelo propuesto por Fausto y col. (Fausto N, Campbell JS, & Riehle KJ, 2006): (1) Factores iniciadores, que hacen competentes a los hepatocitos para responder a los factores de crecimiento y promueven la transición G0/G1; pertenecen a este grupo las citoquinas TNF-α e IL-6; (2) Factores de crecimiento, que permiten a los hepatocitos iniciados o competentes progresar en la transición G1/S; este grupo incluye a los potentes mitógenos HGF, TGF-α y EGF; (3) Comitógenos, que facilitan la acción de los mitógenos, como la insulina y la epinefrina; (4) Inhibidores del crecimiento, que suprimen la respuesta regenerativa de los hepatocitos, cuya expresión está inhibida durante la regeneración; este grupo incluye a la activina y al factor de crecimiento transformante β (TGF-β, del inglés transforming growth factor β); (5) Supresores de los inhibidores de crecimiento, cuya actividad se debe a su elevada afinidad y unión reversible a los inhibidores de crecimiento, incapacitándolos para unirse a sus receptores celulares e impartir sus propiedades; pertenecen a este grupo el inhibidor del TGF-β, el péptido LAP (del inglés latency associated peptide) y el inhibidor de la activina, la folistatina. La Figura 2 muestra un esquema de los factores circulantes que desencadenan la regeneración hepática.
Señales desencadenadas en el hígado luego de una hepatectomía parcial o lesión hepatocelular
FIGURA 2. Factores derivados del intestino (LPS) alcanzan el hígado a través de la sangre portal y activan las células epiteliales y las de Kupffer. Esas últimas elevan la producción de TNFα e IL-6. Otros factores se liberan del páncreas (insulina), duodeno (EGF), glándula adrenal (norepinefrina), glándula tiroides (T3) y lipocitos activados por las células epiteliales (HGF). Estos factores permiten a los hepatocitos pasar de la fase G0 a la G1 y de la G1 a la fase S, lo que conduce a su proliferación. La señalización a través del TGFβ, procedente de los lipocitos, que inhibe la síntesis del ADN, se bloquea durante la fase proliferativa y su actividad se restaura al final del proceso regenerativo para el retorno al estado quiescente. LPS, lipopolisacárico; IL6, interleuquina-6; TNFα, factor de necrosis tumoral alfa; HGF, factor de crecimiento hepatocítico; T3, triyodotiroxina; TGFβ, factor transformante de crecimiento beta; EGF, factor de crecimiento epidérmico.
Cambios hemodinámicos derivados de la HP
La HP de dos tercios elimina quirúrgicamente dos lóbulos hepáticos sin lesión de los residuales. Aunque no hay daño en el tejido residual, hay cambios importantes en los patrones de flujo sanguíneo hepático, lo cual origina grandes cambios en el flujo de sangre que atraviesa el hígado remanente. Este hecho es de enorme importancia e induce un espectro de acontecimientos en todo el hígado que se asemeja a una respuesta de cicatrización de heridas. La vena porta mantiene el flujo completo de sangre procedente del intestino, bazo y páncreas, que atraviesa los sinusoides hepáticos, cuya capacidad, por efecto de la hepatectomía, ha descendido a un tercio de la original. Los sinusoides están tapizados por células endoteliales fenestradas que proporcionan acceso directo del plasma a los hepatocitos. Un estudio en un modelo de shunt porto-hepático, demostró que, si los cambios hemodinámicos se previenen, la activación del HGF es deficiente y se produce apoptosis en los hepatocitos (Marubashi M, Sakon R, Nagano N, Gotoh G, Hashimoto N, & Kubota P, 2004).
El aumento en el flujo de sangre portal trae consigo también mayor disponibilidad de factores de crecimiento y citoquinas procedentes del intestino y páncreas, entre los que se incluyen; insulina, EGF, lipopolisacárido (LPS) y nutrientes derivados de los alimentos (aminoácidos, lípidos y carbohidratos). Los cambios hemodinámicos debidos a la HP también influyen sobre la expresión de los genes tempranos inmediatos (Nakatsuka A, Sokabe M, Yamamoto R & Kamiya S, 2006). Otro aspecto importante es el impacto de la presión parcial de oxígeno en el flujo sanguíneo hepático después de la HP. La sangre portal posee menor concentración de oxígeno que la arterial, así que el incremento relativo en la presión portal ocasiona una disminución en la presión de oxígeno en la sangre circulante, lo cual va a desencadenar una respuesta hipóxica (Khan R, Michalopoulos GK, & Stolz P, 2006).
Los canales de potasio sensibles a ATP y la proteína Kir6.2
Los canales de potasio sensibles a ATP (K-ATP) son hetero-octámeros compuestos por 4 subunidades proteicas Kir6.x (6.1 o 6.2) que forman el poro, y se coensamblan con un receptor sensible a sulfonilurea, formado por 4 subunidades (SUR1 o SUR2) reguladas por las concentraciones intracelulares de ATP y ADP. La propiedad fundamental de los canales K-ATP es que se abren en respuesta a un cambio metabólico, específicamente a una caída del ATP y/o un aumento del ADP. Son canales que producen el eflujo de potasio al espacio extracelular e hiperpolarizan las membranas impidiendo que se activen los canales de calcio. Se encuentran ampliamente distribuidos en diversos tejidos, habiéndose descrito en miocitos cardíacos, células β del páncreas, músculo esquelético, neuronas, músculo liso, riñón y células epiteliales en general (Seino S & Miki T, 2003). Debido a su activación dependiente de la relación ADP/ATP, se constituyen en sensores del estado metabólico de la célula y según ello, regulan la excitabilidad de la membrana celular, por lo que establecen una relación directa entre ambos. Además de acoplar el metabolismo celular con el potencial de membrana, los canales K-ATP pueden regular muchas actividades celulares actuando como sensores metabólicos, especialmente en respuesta a situaciones de estrés metabólico celular tales como hiper o hipoglicemia, isquemia e hipoxia (Seino S & Miki T, 2003).
Canales de K-ATP y daño hepatocelular
Actualmente, se reconoce que la apertura de canales K-ATP podría representar un mecanismo protector contra el daño celular. Por ejemplo, en hígados de ratas sometidos a isquemia-reperfusión, la apertura del canal K-ATP mitocondrial previene la injuria a través de la inhibición de la liberación de citocromo c y la activación de caspasa-3 (Hai S, Takemura S, Minamiyama Y, Yamasaki K, Yamamoto S, Kodai S, Tanaka S, Hirohashi K, & Suehiro S, 2005). La administración de diazóxido (activador de canales de K-ATP mitocondriales) a ratas sometidas a isquemia-reperfusión hepática aumenta la resistencia del hígado al daño isquémico y disminuye la respuesta inflamatoria sistémica. La apertura de K-ATP que induce la despolarización parcial de la membrana mitocondrial, reduce la fuerza impulsora del influjo de Ca2+ durante la isquemia. Dado que la sobrecarga de Ca2+ intracelular puede causar daño mitocondrial, el efecto beneficioso del diazóxido en la lesión por isquemia-reperfusión hepática también puede estar relacionado con la reducción del Ca2+ intracelular de los hepatocitos (Nogueira MA, Coelho AMM, Sampietre SN, Patzina RA, Pinheiro da Silva F, D’Albuquerque LAC & Machado MCC, 2014). En el mismo sentido, se demostró que la administración de diazóxido a ratas sometidas a HP mejora la regeneración hepática al mantener niveles elevados de ATP en el tejido hepático, indicativo de una función mitocondrial mejorada (Nakagawa Y, Yoshioka M, Abe Y, Uchinami H, Ohba T, Ono K & Yamamoto Y, 2012).
En un trabajo previo, mediante la utilización del modelo del ratón knockout en Kir6.2 (Kir6.2-/-), se investigó el rol de los canales Kir6.2/K-ATP en un modelo de injuria hepática inducida por LPS (Du R-H, Tan J, Yan N, Wang L, Qiao C, Ding J-H, & Hu G, 2014). Los autores demostraron que la ausencia de Kir6.2 exacerba la injuria hepática inducida por LPS mediante el aumento de la respuesta inflamatoria mediada por la activación de NF-κB y la inducción de la expresión del inflamasoma NLRP3. En conjunto, todas estas evidencias ponen al canal de K-ATP hepático en un lugar central en la fisiopatología de la enfermedad hepática inflamatoria como también en el mantenimiento del metabolismo energético requerido en los procesos de regeneración hepatocelular. En particular, el canal Kir6.2/K-ATP se perfila como un posible candidato para el tratamiento y/o prevención de la injuria hepática (Du R-H, Tan J, Yan N, Wang L, Qiao C, Ding J-H, & Hu G, 2014). De este modo, emerge la necesidad de avanzar en el conocimiento del rol de Kir6.2 en este tipo de fenómenos.